沖米田 司
RFFLによる形質膜タンパク質品質管理作動機構の解明と CF 創薬への応用
 |
研究代表者 沖米田 司関西学院大学 理工学部 生命医化学科 教授 |
|---|
研究概要
嚢胞性線維症(Cystic Fibrosis; CF)は呼吸器系を侵す単一遺伝病で、世界に8万人の患者が存在する指定難病です(平均寿命40歳)。CFの原因は、形質膜の塩素イオンチャネル CFTR の遺伝子変異(ΔF508 変異)に起因した CFTR タンパク質の形質膜発現低下で、近年、ΔF508 CFTR の形質膜移行を促進する CF治療薬(Orkambi🄬)が上市されましたが、その治療効果が非常に弱く、有効な CF 薬物療法の確立には形質膜で CFTR を安定化する CFTR スタビライザーの開発が望まれています。
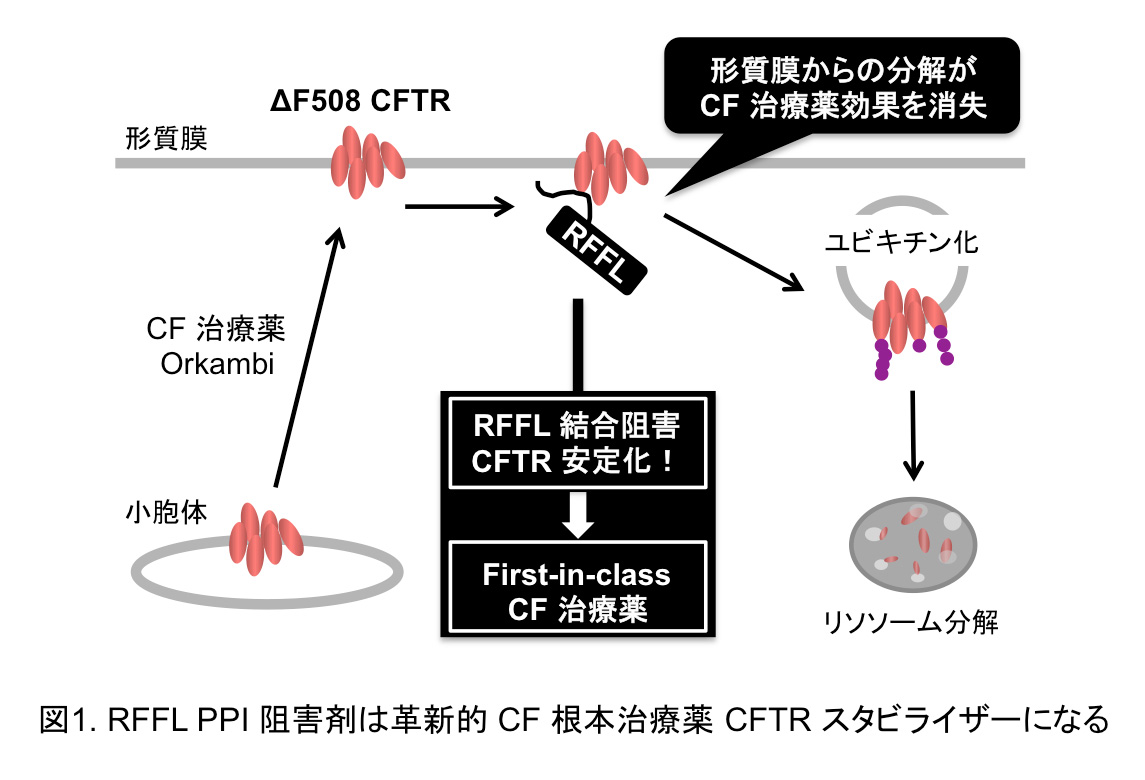
私たちは網羅的siRNA表現型スクリーニングにより、 ΔF508 CFTR の形質膜分解を促進するユビキチンリガーゼ RFFLを同定し、RFFLノックダウン(KD)が CF治療薬 Orkambi🄬 の薬効を増強することを発見しました。RFFL は構造異常を持つ CFTR と直接結合し、異常タンパク質選択的なユビキチン化を促進します。RFFL ノックアウト(KO)マウスは健常であるため、RFFL-CFTR 相互作用(PPI)阻害剤は、形質膜 ΔF508 CFTR を安定化する革新的 CF 根本治療薬 CFTR スタビライザーになる可能性があります(図1、PCT/JP2018/009524 出願)。申請者は、RFFL が E2 酵素 UbcH5c 選択的に変性した ΔF508 CFTRの細胞質領域(ΔF508-NBD1)をユビキチン化することを見出しました。従って、RFFL-UbcH5c PPI 阻害は ΔF508 CFTR のユビキチン化及び形質膜からの分解を阻害し、CF治療薬の有効性を改善することが期待されます。
本研究では、CFTR-RFFL 及び UbcH5c-RFFL PPI機構を明らかにし、本PPIを人工ペプチド(ステープルペプチド等)で人為的に制御する手法を確立します。次に、CFTR-RFFL 及び UbcH5c-RFFL PPI 阻害ペプチドが CFの革新的根本治療薬 CFTR スタビライザーとして、CF治療効果を有するか否かを明らかにします。また、RFFL degrader 等のRFFL機能阻害剤の開発も行い、CFTR スタビライザーとしての有効性を評価します。さらに、形質膜分解シグナルとなる異常CFTR のユビキチンコードを同定し、RFFL KO 細胞インターラクトーム解析により、CFTR エンドサイトーシス及びリソソーム分解を制御するユビキチンデコーダー分子を明らかにします。
研究概要を示す模式図
本領域での研究成果
- Kamada Y, Fukuda R,*Okiyoneda T.
ELISA Based Protein Ubiquitylation Measurement.
Bio-protocol 9, e3430 (2019)
代表的な論文
- Okiyoneda T, Veit G, Dekkers JF, Bagdany M, Soya N, Xu H, Roldan A, Verkman AS, Kurth M, Simon A, Hegedus T, Beekman JM, *Lukacs GL.
Mechanism-based corrector combination restores ΔF508-CFTR folding and function.
Nat. Chem. Biol. 9, 444-454 (2013)
PMID: 23666117 - Bagdany M, Veit G, Fukuda R, Avramescu RG, Okiyoneda T, Baaklini I, Singh J, Sovak G, Xu H, Apaja PM, Sattin S, Beitel LK, Roldan A, Colombo G, Balch W, Young JC, *Lukacs GL.
Chaperones rescue the energetic landscape of mutant CFTR at single molecule and in cell.
Nat. Commun. 8, 398 (2017)
PMID: 28855508 - *Okiyoneda T, Veit G, Sakai R, Aki M, Fujihara T, Higashi M, Susuki-Miyata S, Miyata M, Fukuda N, Yoshida A, Xu H, Apaja PM, Lukacs GL.
Chaperone-Independent Peripheral Quality Control of CFTR by RFFL E3 Ligase.
Dev. Cell 44, 694-708.e7 (2018)
PMID: 29503157 - Fukuda R, *Okiyoneda T.
Peripheral Protein Quality Control as a Novel Drug Target for CFTR Stabilizer.
Front. Pharmacol. 9, 1100 (2018)
PMID: 30319426 - Sakai R, Fukuda R, Unida S, Aki M, Ono Y, Endo A, Kusumi S, Koga D, Fukushima T, Komada M, *Okiyoneda T.
The integral function of the endocytic recycling compartment is regulated by RFFL-mediated ubiquitylation of Rab11 effectors.
J. Cell Sci. 132, jcs228007 (2019)
PMID: 30659120





