鳴海 哲夫
ユビキチン鎖の空間配向制御を指向したケモテクノロジーの開発
 |
研究代表者 鳴海 哲夫静岡大学大学院 総合科学技術研究科 生物有機化学研究室 准教授 |
|---|
研究概要
ユビキチンはC末端グリシン残基が、他のユビキチンのリジン側鎖とイソペプチド結合を形成することでユビキチン鎖を形成し、多種多様な生命現象に関与します。このイソペプチド結合を含む2つのグリシン残基とリジン側鎖からなるユビキチン連結領域は、N末端連結型を除く、全てのユビキチン鎖に含まれる共通構造であり、脱ユビキチン化酵素の認識部位ともなることから、ユビキチン鎖の構造や機能を制御する重要な構造因子です。
近年、化学合成したユビキチン鎖をタンパク質プローブとするユビキチン研究が盛んに行われています。しかし、化学合成したユビキチン鎖の多くは、本来のユビキチン連結領域とは全く異なる構造であるため、天然のユビキチン鎖が取りうる空間配向性やダイナミクス、それらに起因するユビキチン認識を正確に解析することは容易ではありません。また、数種類の非天然型ユビキチン同士を比較した例は皆無であり、ユビキチン連結領域の構造の違いがユビキチン認識に与える影響は、ユビキチン化を起点とする生命現象に影響を及ぼす可能性があります。
これまでに私たちは、タンパク質の普遍的な共通構造であるペプチド結合に着目し、これらを有機化学的に改変した機能性分子を開発し、アミノ酸やペプチドをモダリティとする創薬研究を進めてきました。なかでも、酵素によって容易に加水分解されるペプチド結合を、 結合の長さと角度がよく似た炭素-炭素二重結合に置換したアルケン型ペプチド結合等価体を中心に研究を進め、化学合成法を確立するとともに、様々な生理活性ペプチドに応用することで、加水分解耐性やアミド配座制御能を付与したペプチドミメティックを創出してきました。最近では、これら分子技術をタンパク質の機能解明に応用すべく、タンパク質化学合成との融合研究を進めています。
本研究では、ユビキチン鎖の構造や機能を制御するユビキチン連結領域に着目して、有機化学的手法ならびに計算化学的手法をもとに高機能化したタンパク質プローブ「特殊ユビキチン鎖」を創製することで、ユビキチンの作動機構の理解を加速化するケモテクノロジーの創出を目指します。
研究概要を示す模式図
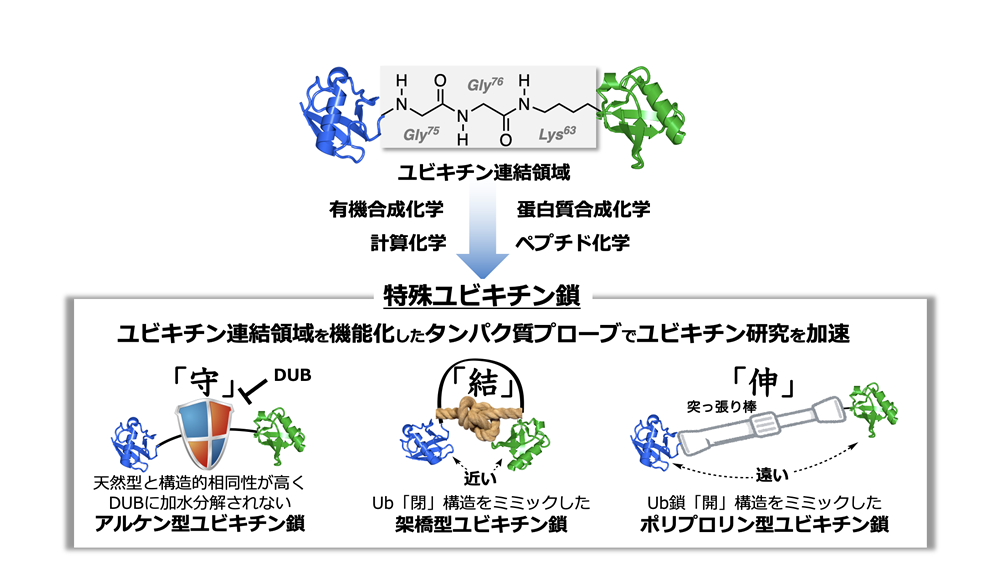
本領域での研究成果
- Kodama Y, Takeo S, Fujimoto J, Sato K, Mase N, *Narumi T.
Synthesis and Structural Characterization of β-Turn Mimics Containing (Z)-Chloroalkene Dipeptide Isosteres.
J. Org. Chem. 87, 2167-2177 (2022)
PMID: 35179382
代表的な論文
- Narumi T, Hayashi R, Tomita K, Kobayashi K, Tanahara N, Ohno H, Naito T, Kodama E, Matsuoka M, *Oishi S, *Fujii S.
Synthesis and biological evaluation of selective CXCR4 antagonists containing alkene dipeptide isosteres.
Org. Biomol. Chem. 8, 616-621 (2009)
PMID: 20090978 - Narumi T, Takano H, Ohashi N, Suzuki A, Furuta T, *Tamamura H.
Isostere-Based Design of 8-Azacoumarin-Type Photolabile Protecting Groups: A Hydrophilicity Increasing Strategy for Coumarin-4-ylmethyls.
Org. Lett. 16, 1184-1187 (2014)
PMID: 24495035 - Kobayakawa T, *Narumi T, *Tamamura H.
Remote Stereoinduction in the Organocuprate-Mediated Allylic Alkylation of Allylic gem-Dichlorides: Highly Diastereoselective Synthesis of (Z)-Chloroalkene Dipeptide Isosteres.
Org. Lett. 17, 2302-2305 (2015)
PMID: 25950639 - Takano T, *Narumi T, Nomura W, Furuta T, *Tamamura H.
Utilization of the Heavy Atom Effect for the Development of a Photosensitive 8-Azacoumarin-Type Photolabile Protecting Group.
Org. Lett. 17, 5372-5375 (2015)
PMID: 26469518 - Kyan R, Sato K, Mase N, *Narumi T.
Pendant Alkoxy Groups on N‐Aryl Substitutions Drive the Efficiency of Imidazolylidene Catalysts for Homoenolate Annulation from Enal and Aldehyde.
Angew. Chem. Int. Ed. 59, 19031-19036 (2020)
PMID: 32662539





