池田 史代
ナノボディーによる標的ユビキチンリガーゼ複合体の細胞内動態の理解と応用
 |
研究代表者 池田 史代大阪大学大学院 生命機能研究科 教授 |
|---|
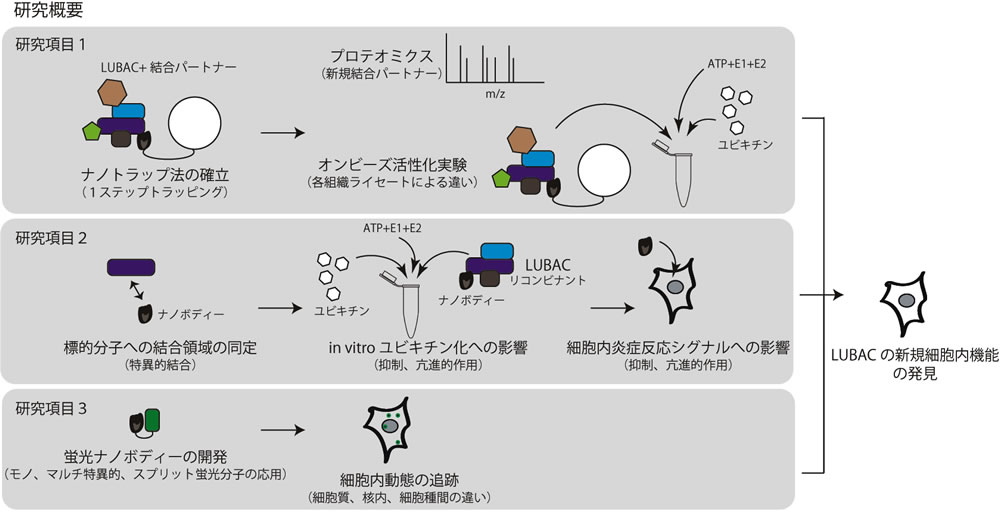
研究概要
生化学的にも構造学的にもユニークな直鎖型ユビキチン鎖は、炎症、選択的オートファジーや免疫制御に重要な役割を果たします。この直鎖型ユビキチン鎖は、ユビキチンリガーゼ複合体LUBACにより誘導され、OTULIN脱ユビキチン化酵素により抑制されます。さらに、7つの分子により特異的に認識されることにより、細胞内でのシグナル伝達に関与します。この様に、直鎖型ユビキチン鎖の作製、抑制、認識を担う主要分子はすでに同定されています。しかしながら、これらの分子の細胞内動態、組織や細胞種特異的なシグナルネットワークの形成とその生物学的効果については不明な部分も多く残されています。例えば、LUBAC構成因子の一つであるHOIL-1Lをコードする遺伝子は自己免疫疾患のみならず、ガンやミオパチーとの相関も示唆されていますが、詳細なメカニズムは不明です。また、これらを解明するのに最適な抗体や分子ツールも存在しないことから、本研究の目的は、申請者のチームが独自に取得した単量体、単一ドメインの小分子であるナノボディーを基盤とした分子ツールの開発とLUBAC の新規制御メカニズムの解明です。そのために、1)各LUBAC 構成因子を抗原とするラマ由来ナノボディークローンの生化学的特徴の解析と分子ツールの開発、2)ナノボディーによるLUBAC活性と生物学的効果への影響の解析、3)ナノボディーによるLUBAC構成因子の細胞内動態の探索、を行います。究極的には、生体内でも組織浸潤性の高いナノボディーの特性を活かして、LUBAC 依存的に引き起こされる疾患コントロールの手法を確立することを目指します。
研究概要を示す模式図
本領域での研究成果
- Rodriguez Carvajal A, Grishkovskaya I, Gomez Diaz C, Vogel A, Sonn-Segev A, Kushwah MS, Schodl K, Deszcz L, Orban-Nemeth Z, Sakamoto S, Mechtler K, Kukura P, Clausen T, *Haselbach D, *Ikeda F.
The linear ubiquitin chain assembly complex (LUBAC) generates heterotypic ubiquitin chains.
eLife 10, e60660 (2021)
PMID: 34142657 - Gomez Diaz C, Jonsson G, Schodl K, Deszcz L, Bestehorn A, Eislmayr K, Almagro J, Kavirayani A, Seida M, Fennell ML, Hagelkrueys A, Kovarik P, Penninger MJ, *Ikeda F.
The ubiquitin ligase HOIL-1L regulates immune responses by interacting with linear ubiquitin chains.
iScience. 24, 103241 (2021)
PMID: 34755089代表的な論文
- Ikeda F, Deribe YL, Skånland SS, Stieglitz B, Grabbe C, Franz-Wachtel M, van Wijk SJ, Goswami P, Nagy V, Terzic J, Tokunaga F, Androulidaki A, Nakagawa T, Pasparakis M, Iwai K, Sundberg JP, Schaefer L, Rittinger K, Macek B, *Dikic I. SHARPIN forms a linear ubiquitin ligase complex regulating NF-κB activity and apoptosis.
- Kumari S, Redouane Y, Lopez-Mosqueda J, Shiraishi R, Romanowska M, Lutzmayer S, Kuiper J, Martinez C, *Dikic I, *Pasparakis M, *Ikeda F. Sharpin prevents skin inflammation by inhibiting TNFR1-induced keratinocyte apoptosis.
- *Rittinger K, *Ikeda F. Linear ubiquitin chains: enzymes, mechanisms and biology.
- Ebner P, Poetsch I, Deszcz L, Hoffmann T, Zuber J, *Ikeda F. The IAP family member BRUCE regulates autophagosome-lysosome fusion.
- Fennell LM, Gomez Diaz C, Deszcz L, Kavirayani A, Hoffmann D, Yanagitani K, Schleiffer A, Mechtler K, Hagelkruys A, Penninger J, *Ikeda F. Site-specific ubiquitination of the E3 ligase HOIP regulates apoptosis and immune signaling.
Nature. 471, 637-641 (2011)
PMID: 21455181
Elife. 3, e03422 (2014)
PMID: 25443631
Open Biol. 7, 170026 (2017)
PMID: 28446710
Nat Commun. 9, 599 (2018)
PMID: 29426817
EMBO J. 39, e103303 (2020)
PMID: 33215740





